合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
基于表面張力的開放式微流體平臺,利用微柱重建三維肺部細胞微環境
來源: BioChip Journal 生物芯片期刊 瀏覽 6 次 發布時間:2024-11-19
人類的肺部由氣管、支氣管和肺泡組成,這些部分是氧氣和養分向人體運輸的重要交換界面。肺部容易發展氣道疾病,因此對其的研究和建模需求日益增加。器官芯片作為一種模擬體外器官細胞微環境的工具,具有成本、倫理、時間和性能等方面的優勢,但制造過程需要整合和選擇復雜的細胞類型、細胞外基質成分和生物制造過程。當前,僅有少數體外微流體平臺能再現肺泡的體內尺寸,且未考慮在氣道炎癥中起重要作用的肺成纖維細胞。傳統的聚二甲基硅氧烷(PDMS)微流體平臺存在低通量和小分子吸附等性能缺陷,限制了大規模生產的可擴展性和整合性。
3D打印為解決這些問題提供了一種解決方案,它提供了與常規PDMS芯片相同的生物性能和生物降解性,同時實現了高通量和無小分子吸附。然而,3D打印的分辨率尚未與軟光刻技術相媲美,且使用固化樹脂無法模擬呼吸運動。近期,某些由昂貴材料制成的設備已經能夠實現幾微米厚度的肺泡所需尺寸,并復制單個肺泡的體內上皮面積,還能模擬呼吸運動。但這些設備不是一次性使用的,在高通量和廣泛應用方面存在不足。因此,仍需進一步研究和改進,以創建更準確、現實和穩健的肺芯片模型。
研究內容
圖1展示了一個基于表面張力的開放式微流體平臺的結構和液體圖案化過程,用于再現肺部的三維細胞微環境。圖1a展示了微流體平臺的頂視圖和側視圖。平臺的中心區域包含微柱陣列,用于形成薄的水凝膠膜,兩側是包含不同細胞懸浮液的流體通道。圖1b展示了水凝膠和不同細胞層的位置安排,模擬肺部細胞環境的氣-液界面結構。圖1c到圖1e展示了圖案化過程的兩個關鍵步驟——液體注入和保持。首先,水凝膠液體通過微柱流動;當液體達到通道的擴展區域時,使用吸取器將多余液體移除,剩余部分被保持在微柱之間形成所需的薄層。這一過程中利用了表面張力的“毛細釘扎”現象,即通過幾何結構和表面特性來控制液體的流動和停留。
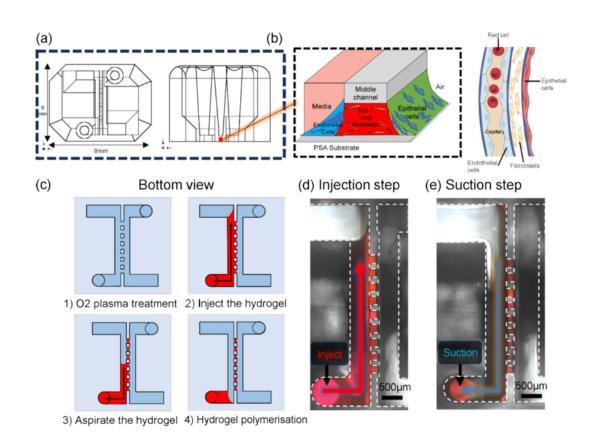
圖1微流控芯片和液體圖案化過程
圖2展示了用于模擬液體填充和圖案化條件的數值模擬和實驗驗證,進一步分析了在微流體平臺中實現毛細釘扎過程的成功條件。圖2a展示了與圖案化成功條件相關的物理參數,包括柱子的高度、間距和側通道的長度。通過這些參數的控制,可以預測液體在微柱之間的保留情況。圖2b展示了液體填充過程的數值模擬,包括在不同接觸角(例如60°和120°)條件下的液體流動和釘扎效果。模擬結果顯示了如何通過改變接觸角和壓力控制液體在微柱之間的流動和停留。圖2b的模擬驗證了在較大接觸角下液體被釘扎在微柱邊緣的效果。圖2c至2e總結了不同微柱高度、間距和側通道長度對液體保留過程的影響,通過這些參數優化可實現液體在微柱之間的穩定釘扎,適用于后續的細胞培養實驗。
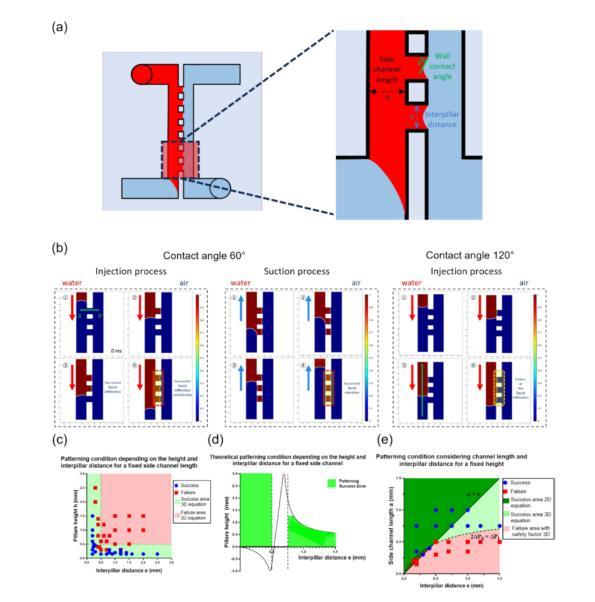
圖2數值模擬與圖案化條件
圖3通過細胞加載流程示意圖和熒光圖像,展示了微流體平臺在再現肺泡三維微環境方面的有效性。圖3a展示了細胞加載的步驟,包括在水凝膠薄膜兩側加入不同類型的細胞,以創建多層細胞結構。圖3b和3c展示了微流體平臺上與內皮細胞和肺成纖維細胞的共培養熒光圖像。水凝膠薄膜中含有橙色染色的成纖維細胞,水凝膠膜側面綠色層表示生長的內皮細胞層。這種結構模擬了肺部的基質和內皮層,為后續肺部疾病研究提供了生理相關的模型。圖3d和3e分別展示了細胞配置的示意圖和最大投影的共聚焦顯微圖像。在這些圖中可以看到肺成纖維細胞(橙色)和內皮細胞(綠色)在水凝膠薄膜的不同層次的分布情況,形成了一個三維的細胞共培養環境。圖像還顯示,細胞在培養過程中保持了較高的活力,并成功地在水凝膠薄膜周圍形成了均勻的細胞層。
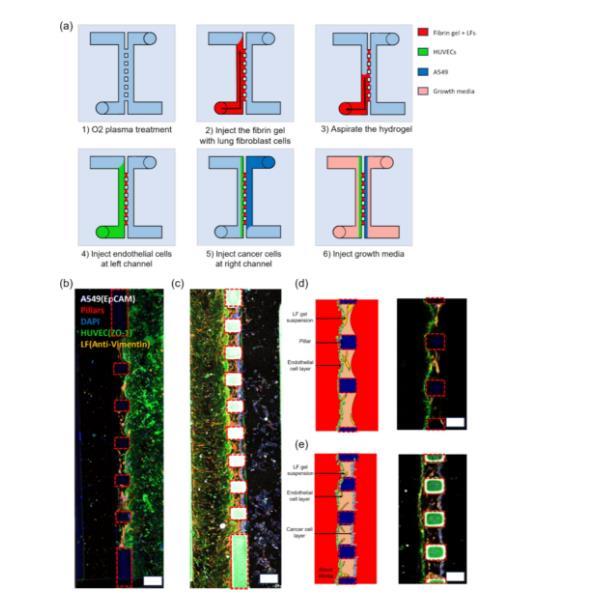
圖3芯片的共培養和三培養
總結與展望
在這項研究中展示了3D打印和毛細釘固著作為制造高通量微流體設備的有效工具的潛力。結果表明,工程化一個薄的水凝膠層以模擬氣-液界面的大小是可行的,這個大小接近100-150微米,適合細胞培養,并具有多種細胞圖案配置,便于共聚焦成像。未來的工作可以包括開發一個完整的雙細胞層模型,其中包括癌細胞,或使用空氣泵模擬設備內的呼吸。這種微流體平臺提供了一系列廣泛的未來應用,例如粉末吸入實驗或藥物篩選。










