合作客戶/
拜耳公司 |
同濟大學 |
聯(lián)合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關(guān)新聞Info
推薦新聞Info
-
> 強紫外線輻射對減縮劑抑制水泥石干縮變形效果研究(一)
> 無機粒子對TPAE界面張力、發(fā)泡、抗收縮行為的影響(四)
> 無機粒子對TPAE界面張力、發(fā)泡、抗收縮行為的影響(三)
> 無機粒子對TPAE界面張力、發(fā)泡、抗收縮行為的影響(二)
> 無機粒子對TPAE界面張力、發(fā)泡、抗收縮行為的影響(一)
> 弱堿三元采出液油水界面動態(tài)界面張力、強度、等特性研究
> 植保無人機噴頭和噴霧助劑對藥液表面張力、霧滴密度、覆蓋率的影響(二)
> 植保無人機噴頭和噴霧助劑對藥液表面張力、霧滴密度、覆蓋率的影響(一)
> 無人機噴霧作業(yè)下荔枝葉片上的表面張力、接觸角及霧滴沉積特性
> 不同界面張力-潤濕性組合的滲吸液體系對于化學滲吸效果的影響規(guī)律
應(yīng)用不同組裝的磷脂酰膽堿對牛精漿蛋白的隔離:一種新的技術(shù)方法——結(jié)果和討論
來源:上海謂載 瀏覽 874 次 發(fā)布時間:2021-12-20
3.結(jié)果
3.1.精漿的界面性質(zhì)
精漿SDS-PAGE電泳顯示存在一系列不同比例的14至120 kDa的多肽(圖1),與先前的研究結(jié)果一致[37]。在車道4上估計了14至30 kDa之間的五個主要波段的比例。
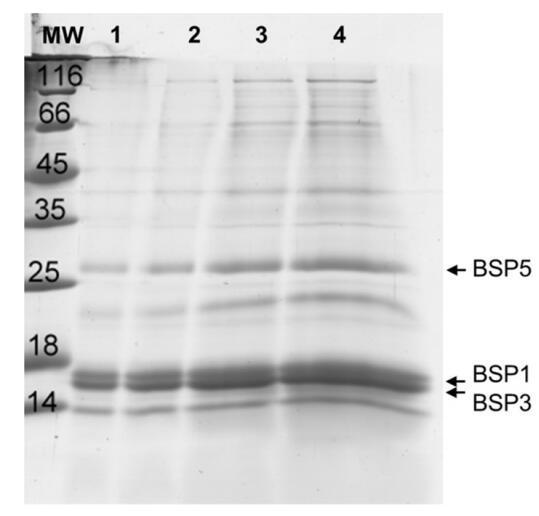
圖1。從牛射精中分離并以不同濃度沉積的精漿SDS-PAGE凝膠:lane 1:1μg;泳道2:2μg;泳道3:5μg和泳道4:10μg。
在大約16–17 kDa(74%強度)處發(fā)現(xiàn)了兩條非常緊密和強烈的條帶。它們被歸因于BSP1和BSP3[12]。在大約28 kDa(9%)處檢測到第二條帶,對應(yīng)于BSP5[12]。BSP1、BSP3和BSP5代表精漿中所含最小多肽的83%(在整個提取物中約占65%)[17]。另一條帶在22kDa(4%)處檢測到,另一條帶在14kDa(13%)處檢測到,對應(yīng)于核糖核酸酶[22]。
通過跟蹤精漿水溶液的表面張力(圖2)與濃度(吉布斯膜),突出了這些組分的表面活性。新樣品的表面張力相對較低(47 mN/m),并隨著樣品的稀釋而增加。在1/100000的大稀釋后,表面張力值等于純緩沖-空氣界面(72 mN/m)的值。因此,精漿顯示出顯著的表面活性:首先,新鮮樣品(47 mN/m)的表面張力與已知表面活性蛋白(如牛血清白蛋白[38]或溶菌酶[39])的值一樣低,其次,表面活性仍然存在于較大的濃度范圍內(nèi)(需要稀釋100000以去除表面活性)。此外,通過朗繆爾薄膜分析了空氣-緩沖界面處表面薄膜的穩(wěn)定性。薄膜的壓縮等溫線(圖3)顯示壓力在兩個步驟中從0顯著增加到35 mN/m。在18.9 mN/m時,出現(xiàn)斜率斷裂,這與空氣-緩沖界面分子構(gòu)象的變化有關(guān)。在較高壓力下壓縮膜的能力(大約與生物膜相關(guān)的壓力,25 mN/m)表明,由精漿成分形成的膜具有較高的穩(wěn)定性。
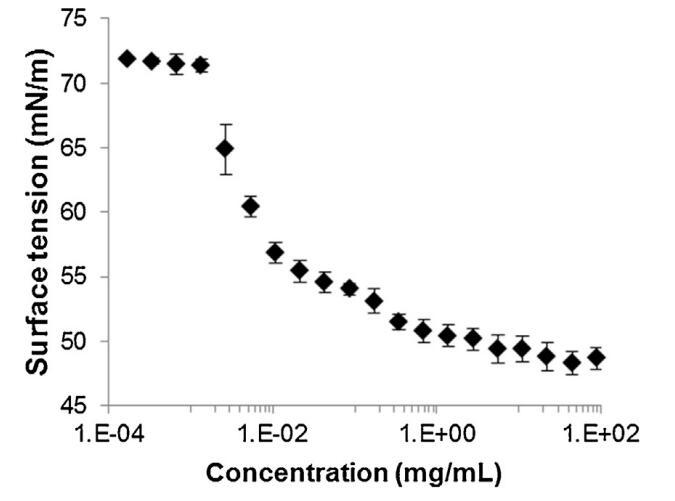
圖2。牛精漿溶液在空氣-水界面處的表面張力(±標準偏差),與提取物中所含蛋白質(zhì)的濃度有關(guān),并以對數(shù)標度表示(T=23.2℃±0.3℃,n=2,每個樣品重復4次)。
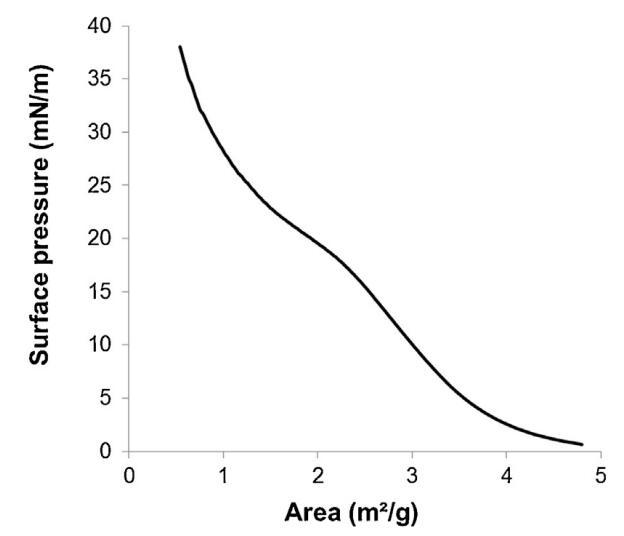
圖3。通過傳播精漿在空氣/緩沖液界面形成的單層的表面壓力面積(π–A)等溫線(n=3,標準偏差在0-18.9 mN/m范圍內(nèi)不超過1.5 mN/m,在18.9-38 mN/m范圍內(nèi)不超過1.2 mN/m)。
3.2.低密度脂蛋白和脂質(zhì)體對精子膜仿生外小葉的作用
將低密度脂蛋白和脂質(zhì)體引入精子膜仿生外小葉亞期的影響如圖4所示。對于控制測量(未注入任何保護劑,設(shè)計為圖4中的M),表面積隨時間略微減小。當?shù)兔芏戎鞍妆蛔⑸涞街亟ǖ耐庑∪~下方的亞相(圖4中的曲線M/LDL)時,它導致表面積快速而大的增加。相反,與參考單層(曲線M)相比,脂質(zhì)體的注射(圖4中的曲線M/C4)幾乎沒有改變單層的膜壓力。脂質(zhì)體與單層脂質(zhì)體的結(jié)合動力學比低密度脂蛋白慢得多。因此,在與精液制備相對應(yīng)的時間尺度上,脂質(zhì)體在空氣-水界面上的吸附較弱。
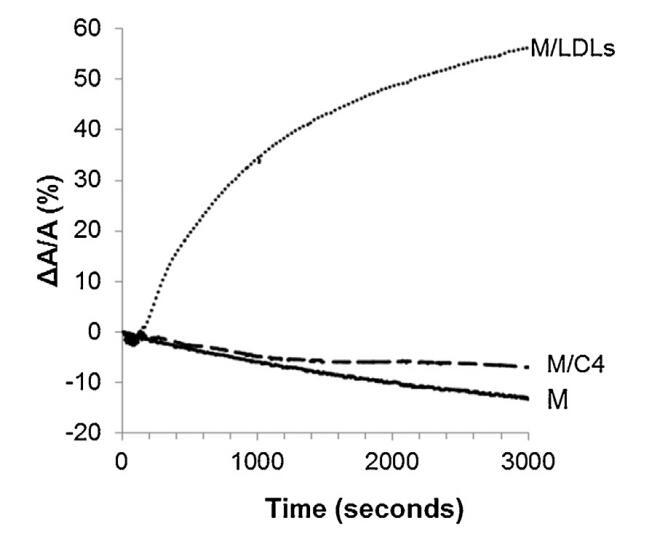
圖4。單層(M)所覆蓋的界面的相對表面積隨時間的變化,該單層(M)以25 mN/M的速度壓縮,并在不含任何額外分子(-)的緩沖液上形成,(…)LDL(4.6 mg PC)和(-)脂質(zhì)體C4(含4.8 mg PC)。空氣-緩沖界面處的溫度為34℃。
對于低密度脂蛋白,根據(jù)低密度脂蛋白的組成,注射磷脂酰膽堿的量估計為4.6毫克[33]。就脂質(zhì)體而言,該分散體含有6.55±0.02 mg脂質(zhì),即4.8 mg磷脂酰膽堿。在重建的精子膜外小葉下注射低密度脂蛋白后,表面積的大幅增加可能與低密度脂蛋白在空氣-水界面自發(fā)吸附和擴散的能力有關(guān)[33]。低密度脂蛋白在界面處的容易破壞可能釋放出磷脂和蛋白質(zhì),這些磷脂和蛋白質(zhì)是表面活性物質(zhì),而甘油三酯是不可溶的[33]。對于脂質(zhì)體,形成雙層磷脂和形成單層磷脂之間的平衡取決于鏈不飽和度、鏈長和極性頭基[40]。考慮到雞蛋卵磷脂(PC 74%)的主要成分及其脂肪酸組成[41],飽和PC和不飽和PC的比例分別約為48%和52%。在本研究的溫度下,飽和PC未熔化,可能不會在界面擴散,而不飽和PC遠遠超過其熔化溫度,并可能擴散。在剩余的部分PE(11%)中,形成磷脂的雙層和單層之間的平衡與磷脂的結(jié)構(gòu)密切相關(guān),因此不能對它們給出任何結(jié)論。因此,沒有基本的解釋。雞蛋脂質(zhì)體缺乏吸附可以解釋為其擴散之前已在自由界面上進行過檢查:界面上已經(jīng)存在的單層可能會限制磷脂基脂質(zhì)體的擴散,而磷脂基脂質(zhì)體在其他地方被認為是高穩(wěn)定性的散裝物,尤其是由磷脂酰膽堿組成時。
3.3.低密度脂蛋白和脂質(zhì)體分離精漿成分
將牛精漿(SP)注射到單層下方時,監(jiān)測分子面積隨時間的變化(圖5中的曲線M/SP)。由于脂質(zhì)覆蓋了界面,表面積并沒有立即增加,而是在150s后才增加。它在150秒內(nèi)達到最大值(注射后300秒),然后穩(wěn)定300秒并隨時間緩慢下降(圖5)。表面積的快速增加表明SP組分(很可能是蛋白質(zhì))具有良好的表面活性,如圖所示。2和3。600秒后,比表面積的減小速度與純單分子膜相同。因此,BSP蛋白一旦被吸附,就會留在界面上。
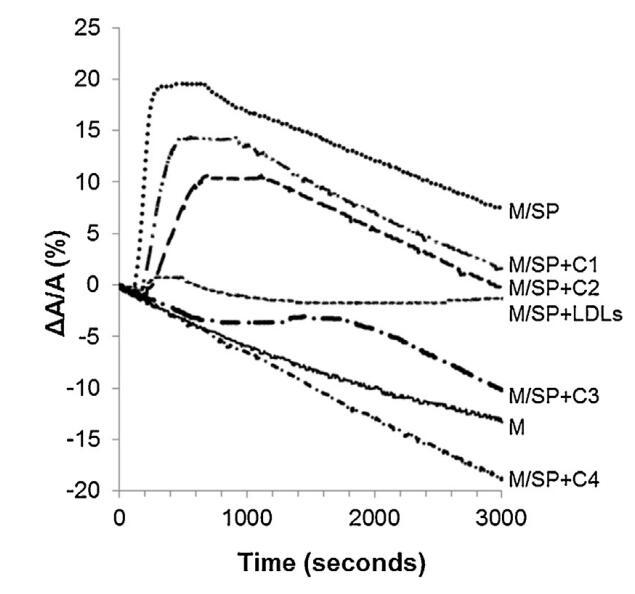
圖5。注入(…)后,由單層(M)覆蓋并在不含(-)額外分子的緩沖液上形成的界面的相對表面積隨時間的變化SP(26.6±1.5 mg蛋白質(zhì))、SP(26.6±1.5 mg蛋白質(zhì))和不同濃度(··-)C1、(·-)C2的脂質(zhì)體的混合物,(·-)C3和(·-)C4(分別為1.17±0.02 mg、2.18±0.02 mg、4.37±0.02 mg和6.55±0.02 mg脂質(zhì))和(---)LDL(4.6 mg PC)和SP(26.6±1.5 mg蛋白質(zhì))的混合物。空氣-緩沖界面處的溫度為34℃。表面壓力保持在25 mN/m。
當LDL與牛精漿以重量-蛋白質(zhì)比10:1(BSP:LDL)混合并注射到單層下方時,隨時間記錄的單層分子面積幾乎沒有變化(曲線M/SP+LDL,圖5)。400秒左右出現(xiàn)一個肩部,顯示BSP蛋白的弱吸附(該肩部代表M/SP的5%,上圖曲線)。然后,分子面積的變化在1000秒后減小并趨于穩(wěn)定。其下降幅度不如M和M/SP曲線的變化幅度大,表明LDL組分吸附,與它們在界面上的高擴散能力一致(曲線M/LDL,圖4)。因此,由于低密度脂蛋白(LDL),SP中BSP蛋白在界面上的吸附大大減少,BSP/LDL的比率非常接近最佳值,以完全防止BSP蛋白影響單層。根據(jù)低密度脂蛋白的組成,注射磷脂酰膽堿的量估計為4.61毫克[33]。因此,向4.61 mg低密度脂蛋白磷脂酰膽堿注射26.6 mg精漿蛋白質(zhì),即0.17 mg磷脂酰膽堿注射1 mg精漿蛋白質(zhì)。
脂質(zhì)體(不同濃度)對BSP蛋白的作用也如圖5所示。脂質(zhì)體在進入亞階段前與精漿接觸。隨著脂質(zhì)體中濃度的增加(曲線M/SP+C1至C4),BSP蛋白吸附引起的表面積增加逐漸延遲并減少。當含量達到4.37 mg(C3)時,界面上仍有少量BSP蛋白摻入,1600 s時出現(xiàn)肩部。在最高濃度(C4)下,未觀察到BSP蛋白摻入,分子面積的變化甚至比對照曲線更負,表明膜組分在亞相中輕微溶解。因此,脂質(zhì)體作用于BSP蛋白的方式與LDL相同。最有趣的比例似乎介于C3和C4之間。根據(jù)確定面積變化與脂質(zhì)體注射磷脂質(zhì)量之間相互作用的曲線計算得出(圖6)。注射26.6 mg BSP的最佳質(zhì)量為4.6 mg,即PC:BSP比為0.16(w/w)。
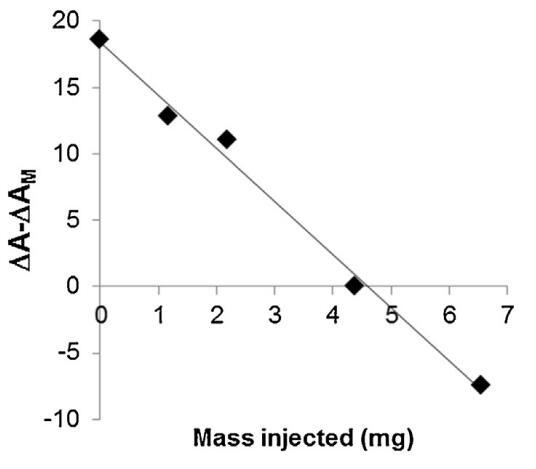
圖6。相對面積隨注射到亞相的脂質(zhì)體質(zhì)量的變化。線性回歸的R2為0.992。
3.4.脂質(zhì)體對精漿作用的顯微評價
用透射電鏡(TEM)觀察脂質(zhì)體或LDL與含有SP的BSP蛋白的混合物,并與對照組進行比較。無論放大倍數(shù)如何,與精漿相對應(yīng)的圖像均未顯示任何結(jié)構(gòu)(圖S1)。相反,與LDL和脂質(zhì)體相關(guān)的結(jié)構(gòu)很容易通過(i)LDL的致密且相當圓的形狀(圖7A)和(ii)脂質(zhì)體的圓形且有時為多層結(jié)構(gòu)(圖7B)來識別。在存在精漿的情況下,對整套圖像的分析仍然顯示出圓形物體。它們的大小平均與未使用螯合劑分析的大小相似(圖S2)。然而,在SP存在的幾個地方,觀察到一些大的圓形物體,其特征是(i)被厚層(圖7C含LDL)包圍的天然狀結(jié)構(gòu),或(ii)環(huán)形內(nèi)的致密核心(圖7D含脂質(zhì)體和圖S3)。與圖7B相比,與精漿混合的脂質(zhì)體系統(tǒng)地呈現(xiàn)出比天然脂質(zhì)體更致密的核心。這些新結(jié)構(gòu)可能是由于BSP蛋白滲透到界面層而導致膜破裂的結(jié)果,從而導致TEM對比度的改變。

圖7。(A)低密度脂蛋白,(B)脂質(zhì)體,(C)低密度脂蛋白和精漿(精漿中的比例為0.17 mg PC/mg BSP蛋白質(zhì))和(D)脂質(zhì)體和精漿(精漿中的比例為0.16 mg PC脂質(zhì)體/mg BSP蛋白質(zhì))的冷凍電鏡圖像。
4.討論
4.1.BSP蛋白的表面性質(zhì)及其可能的生物學作用
張力測定結(jié)果顯示精漿中含有表面活性成分。這些很可能是蛋白質(zhì),因為它們構(gòu)成精漿的主要部分。它們由幾個親水性和疏水性域組成[5],賦予它們兩親性。考慮到生物學背景,我們可以假設(shè)BSP蛋白能夠到達磷脂覆蓋的界面,這是由于它們與PC的相互作用和自身的表面活性。這可以解釋為什么這個過程很快[42]。將肽或蛋白質(zhì)插入磷脂單分子膜通常在比凝聚域更可壓縮的流體域中進行[43]。在34°C時,液域由血漿鹵素和不飽和磷脂酰膽堿組成[35]。因此,根據(jù)前面提到的涉及疏水腔的機制,BSP蛋白可以很容易地穿透這些流體結(jié)構(gòu)域,在這些流體結(jié)構(gòu)域中它們可以立即與含有磷酸膽堿的分子相互作用[11,12,34,42,44–46]。吸附的BSP量可能受到流體域可壓縮性的限制。綜上所述,BSP蛋白質(zhì)一旦被吸附,由于其表面性質(zhì)(我們的工作)、構(gòu)象重排[47]以及它們與膜組件的強烈相互作用[48],仍然固定在界面上。
4.2.脂質(zhì)體和低密度脂蛋白在分離BSP蛋白中的作用
我們的結(jié)果表明,只要使用合適的脂質(zhì)體/BSP比例,脂質(zhì)體就可以像LDL一樣有效地阻止BSP蛋白到達界面。對于低密度脂蛋白,我們的模型顯示,低溫保存中常用的BSP/LDL比率(10:1 w/w)非常接近最佳值,以完全防止BSP蛋白影響單層。低密度脂蛋白組織中PC/BSP與PC的比率為0.17 mg磷脂酰膽堿,1 mg精漿蛋白質(zhì)。同樣,脂質(zhì)體的最佳比例PC/BSP為0.16 mg磷脂酰膽堿和1 mg精漿蛋白質(zhì)。知道卵子中PC的比例可能取決于喂食情況,不同批次的LDL中PC的比例可能不同,因此這些比例被認為是相等的。該比率與LDL或脂質(zhì)體的隔離結(jié)構(gòu)無關(guān)的事實表明,LDL中的載脂蛋白不與BSP結(jié)合,盡管這種結(jié)合是可能的[26,49]。更引人注目的是,這一結(jié)果表明PC作為LDL中的單層或脂質(zhì)體中的雙層組裝沒有影響。在低密度脂蛋白的情況下,磷脂占據(jù)外層單層,并且所有這些磷脂都可被蛋白質(zhì)接近。相反,只有形成單層脂質(zhì)體的雙層外小葉的磷脂真正與BSP蛋白直接接觸。由于脂質(zhì)體和低密度脂蛋白的絡(luò)合比率相同,并且PCP分子(74%)也構(gòu)成雙層的內(nèi)小葉,因此這些分子也參與BSP蛋白的絡(luò)合。與BSP蛋白易于插入疏水膜相一致,這些BSP蛋白可向內(nèi)小葉遷移,并誘導脂質(zhì)體雙層破裂/融合,如TEM所觀察到的。然而,樣品中LDL和脂質(zhì)體的結(jié)構(gòu)變化并不普遍,BSP蛋白可以認為主要錨定在LDL和脂質(zhì)體的表面。當脂質(zhì)體與BSP的比例高于本文所研究的比例時,BSP1(BSP家族中的主要蛋白質(zhì))誘導脂質(zhì)小泡的伸長和珠項鏈狀結(jié)構(gòu)的形成,這些結(jié)構(gòu)演變?yōu)樾∨莼蚓€狀結(jié)構(gòu)[50]。










